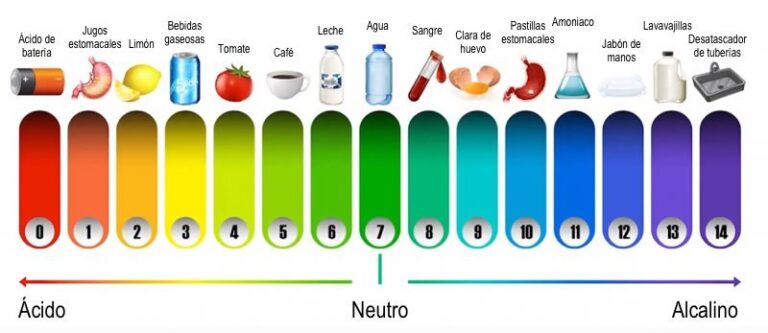
El pH es una medida que indica la acidez o alcalinidad de una sustancia. Se expresa en una escala numérica que va desde 0 hasta 14, donde:
- Un pH menor a 7 indica que la sustancia es ácida.
- Un pH igual a 7 indica que la sustancia es neutra.
- Un pH mayor a 7 indica que la sustancia es alcalina o básica.
El valor exacto del pH de una sustancia se obtiene mediante una prueba con un medidor de pH o mediante cálculos químicos. Es importante tener en cuenta que el pH puede afectar diferentes procesos químicos, biológicos y ambientales.
Por ejemplo, el pH del agua es crucial para la vida acuática, ya que muchas especies solo pueden sobrevivir en un rango de pH específico. En el cuerpo humano, el pH de la sangre se mantiene en un estrecho margen alrededor de 7,4 para garantizar un funcionamiento adecuado de las células y los órganos.
Definición y concepto básico del pH
El pH es un concepto fundamental en química que mide el grado de acidez o alcalinidad de una sustancia. Se refiere a la concentración de iones de hidrógeno presentes en una disolución y se expresa en una escala numérica que va de 0 a 14.
En términos simples, el pH indica si una sustancia es ácida, neutra o alcalina. Un valor de pH inferior a 7 indica acidez, un valor de 7 es neutro y un valor superior a 7 indica alcalinidad. Por ejemplo, el agua pura tiene un pH de 7, lo que la clasifica como neutra.
La fórmula matemática para calcular el pH es:
pH = -log[H+]
Donde [H+] representa la concentración de iones de hidrógeno en la solución. Cuanto mayor sea la concentración de iones de hidrógeno, más ácida será la sustancia y menor será su valor de pH.
Importancia del pH en la vida cotidiana
Entender el concepto de pH es crucial en diversos campos, desde la industria alimentaria hasta la medicina. Por ejemplo, en la agricultura, el pH del suelo es fundamental para determinar qué cultivos pueden crecer de manera óptima en una determinada área. Un suelo demasiado ácido o alcalino puede afectar negativamente la salud de las plantas.
En el cuerpo humano, mantener un equilibrio adecuado de pH es esencial para el funcionamiento óptimo de procesos fisiológicos. La sangre, por ejemplo, tiene un pH ligeramente alcalino de aproximadamente 7,4. Cualquier desviación significativa de este valor puede ser peligrosa y afectar la salud.
Consejos para medir y regular el pH
- Utiliza tiras reactivas de pH para medir el nivel de acidez o alcalinidad de una sustancia. Estas tiras cambian de color según el pH de la solución.
- Ajusta el pH de la piscina utilizando productos químicos específicos para garantizar un agua limpia y segura para el baño.
- Consulta a un profesional de la salud si tienes dudas sobre el impacto del pH en tu cuerpo y cómo mantener un equilibrio adecuado.
El pH es un indicador clave que nos permite comprender la naturaleza ácida o alcalina de una sustancia y su importancia en diversos aspectos de nuestra vida diaria.
La escala del pH: cómo se mide y qué significa
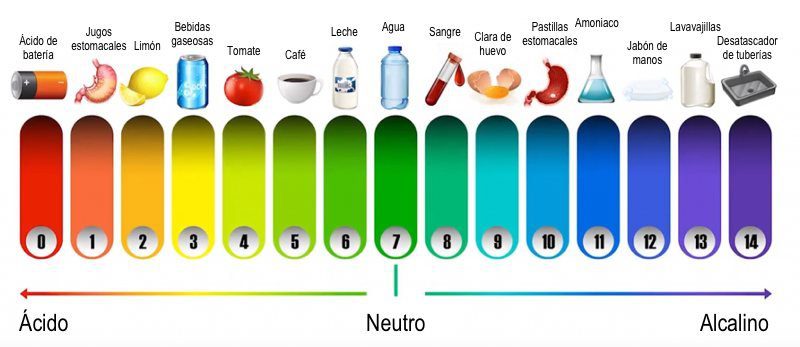
La escala del pH es una herramienta fundamental en química para medir la acidez o alcalinidad de una sustancia. Esta escala va desde 0 hasta 14, donde 0 indica una alta acidez, 7 representa la neutralidad y 14 corresponde a una alta alcalinidad. Cuanto más bajo sea el número en la escala del pH, más ácida es la sustancia, y a medida que el número aumenta, la sustancia se vuelve más alcalina.
Para entender cómo se mide el pH de una sustancia, es esencial conocer el concepto de iones de hidrógeno (H+). En soluciones acuosas, la concentración de iones de hidrógeno determina el pH. Si la concentración de H+ es alta, el pH será bajo y la sustancia será ácida. Por el contrario, si la concentración de H+ es baja, el pH será alto, lo que indica alcalinidad.
La fórmula para calcular el pH de una sustancia es:
pH = -log[H+]
Por ejemplo, si la concentración de iones de hidrógeno en una solución es de 1×10-4 M, el cálculo del pH sería:
pH = -log(1×10-4) = 4
En este caso, el pH de la solución sería 4, lo que indica que es ácida.
El papel del pH en el cuerpo humano y su importancia
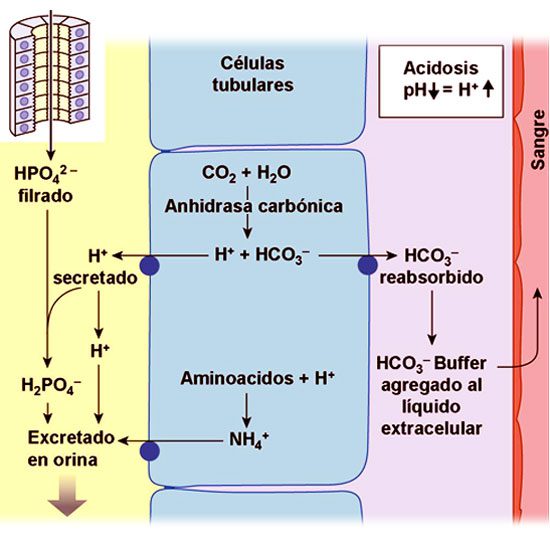
El pH es una medida que indica el nivel de acidez o alcalinidad de una sustancia. En el cuerpo humano, el equilibrio del pH es fundamental para el funcionamiento adecuado de diversas funciones biológicas. El rango de pH en el cuerpo varía según la parte del organismo que se esté considerando. Por ejemplo, el pH del estómago es ácido (alrededor de 1.5 a 3.5) debido a los ácidos gástricos necesarios para la digestión de los alimentos, mientras que la sangre tiene un pH ligeramente alcalino, en torno a 7.35 a 7.45.
El mantenimiento del equilibrio del pH en el cuerpo es crucial para la salud y el bienestar general. Cuando el pH se desvía de los valores normales, pueden surgir problemas de salud. Por ejemplo, la acidosis (cuando el cuerpo se vuelve demasiado ácido) o la alcalosis (cuando el cuerpo se vuelve demasiado alcalino) pueden tener efectos adversos en el funcionamiento de órganos vitales. Por tanto, es vital mantener un adecuado equilibrio de pH para garantizar un óptimo funcionamiento del organismo.
Importancia de mantener el equilibrio del pH en el cuerpo
El equilibrio del pH en el cuerpo es esencial para múltiples procesos biológicos, entre los que se incluyen:
- Funcionamiento adecuado de enzimas y proteínas: muchas enzimas y proteínas biológicas requieren un pH específico para poder llevar a cabo sus funciones de manera óptima. Cualquier desviación significativa del pH óptimo puede afectar negativamente su actividad.
- Transporte de sustancias: el pH influye en la capacidad de las membranas celulares para transportar diferentes sustancias, como nutrientes y desechos. Un desequilibrio en el pH puede interferir en este proceso vital para la vida.
- Regulación de la presión osmótica: el equilibrio del pH es crucial para mantener la presión osmótica adecuada dentro y fuera de las células. Esto es fundamental para evitar la hinchazón o deshidratación celular.
El pH desempeña un papel fundamental en el funcionamiento adecuado del cuerpo humano. Mantener un equilibrio adecuado de pH a través de una dieta equilibrada, hidratación adecuada y un estilo de vida saludable es esencial para promover la salud y prevenir posibles complicaciones relacionadas con desequilibrios ácido-base.
Factores que pueden alterar el pH y sus consecuencias
Los factores que pueden alterar el pH de una sustancia son diversos y es fundamental comprender cómo afectan a su valor. Algunos de los elementos que pueden influir en el pH incluyen la adición de sustancias ácidas o básicas, la temperatura, la presión y la concentración de iones en la solución.
Por ejemplo, si se añade ácido clorhídrico (HCl) a una solución acuosa, se incrementará la concentración de iones de hidrógeno (H+) en el medio, lo que resultará en una disminución del pH. Por otro lado, si se agrega hidróxido de sodio (NaOH), se aumentará la concentración de iones de hidroxilo (OH-) y, en consecuencia, el pH se elevará, volviéndose más básico.
La temperatura también puede afectar el pH de una sustancia, ya que algunos compuestos químicos pueden experimentar cambios en su acidez o basicidad a medida que se calientan o enfrían. Por ejemplo, el agua pura a 25°C tiene un pH de 7, pero a temperaturas más altas, puede disociarse parcialmente en iones de hidrógeno y oxígeno, alterando su pH.
Consecuencias de la alteración del pH
Las consecuencias de una variación en el pH pueden ser significativas, tanto en el ámbito químico como en el biológico. En sistemas biológicos, como el cuerpo humano, mantener un pH equilibrado es crucial para el funcionamiento adecuado de enzimas, proteínas y otras moléculas. Por ejemplo, un cambio brusco en el pH sanguíneo puede llevar a condiciones peligrosas como la acidosis o la alcalosis.
En el caso de suelos agrícolas, un pH inadecuado puede afectar la disponibilidad de nutrientes para las plantas, limitando su crecimiento y desarrollo. Por ello, es fundamental realizar análisis de suelos de forma periódica para ajustar el pH según las necesidades de los cultivos.
En el ámbito industrial, la variación del pH puede influir en la eficacia de procesos químicos y en la calidad de los productos finales. Por ejemplo, en la fabricación de productos farmacéuticos, es esencial controlar con precisión el pH para garantizar la estabilidad y eficacia de los medicamentos.
Preguntas frecuentes
¿Qué es el pH?
El pH es una medida de la acidez o alcalinidad de una sustancia, que va de 0 a 14.
¿Cuál es el valor neutro de pH?
El valor neutro de pH es 7, lo que indica un equilibrio entre acidez y alcalinidad.
¿Qué indica un pH menor a 7?
Un pH menor a 7 indica que la sustancia es ácida, siendo 0 el valor más ácido.
¿Y qué significa un pH mayor a 7?
Un pH mayor a 7 indica que la sustancia es alcalina, siendo 14 el valor más alcalino.
¿Cómo se calcula el pH?
El pH se calcula mediante la concentración de iones de hidrógeno en una sustancia, utilizando la fórmula: pH = -log[H+].
¿Por qué es importante medir el pH?
Es importante medir el pH porque muchas reacciones químicas, procesos biológicos y calidad del agua dependen de un equilibrio específico de acidez y alcalinidad.
¿Cómo afecta el pH a los seres vivos?
El pH puede afectar la salud de los seres vivos, ya que un desequilibrio puede causar problemas en el funcionamiento de enzimas y otros procesos biológicos.
- El pH es una medida de la acidez o alcalinidad de una sustancia.
- El valor neutro de pH es 7.
- Un pH menor a 7 indica acidez, mientras que un pH mayor a 7 indica alcalinidad.
- El pH se calcula mediante la concentración de iones de hidrógeno en una sustancia.
- Es importante medir el pH para controlar procesos químicos, biológicos y la calidad del agua.
- Un desequilibrio en el pH puede afectar la salud y el funcionamiento de los seres vivos.
¡Déjanos tus comentarios y revisa otros artículos sobre química y biología en nuestra web para seguir aprendiendo!