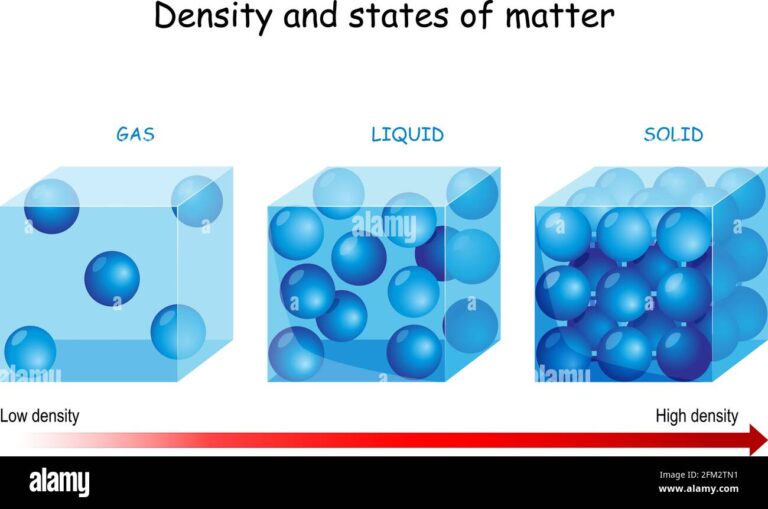
Las sustancias químicas se pueden clasificar según su estado físico en tres categorías principales: sólidas, líquidas y gaseosas. A continuación, se detalla la clasificación de las sustancias químicas de acuerdo a su estado físico:
Sustancias sólidas:
Las sustancias sólidas se caracterizan por tener una forma y un volumen definidos. Las partículas que componen las sustancias sólidas están muy cerca unas de otras y tienen una estructura ordenada. Algunos ejemplos de sustancias químicas sólidas son la sal de mesa, el azúcar o el hierro.
Sustancias líquidas:
Las sustancias líquidas no tienen una forma definida, pero sí un volumen constante. Las partículas que forman las sustancias líquidas están más separadas que en los sólidos, lo que les permite fluir y adaptarse al recipiente que las contiene. Ejemplos de sustancias químicas líquidas son el agua, el alcohol o el aceite.
Sustancias gaseosas:
Las sustancias gaseosas no tienen una forma ni un volumen definido, ya que ocupan todo el espacio disponible en el recipiente que las contiene. Las partículas que constituyen las sustancias gaseosas están muy separadas unas de otras y se mueven en todas direcciones. Algunos ejemplos de sustancias químicas gaseosas son el oxígeno, el dióxido de carbono o el gas natural.
Definición y características de las sustancias químicas
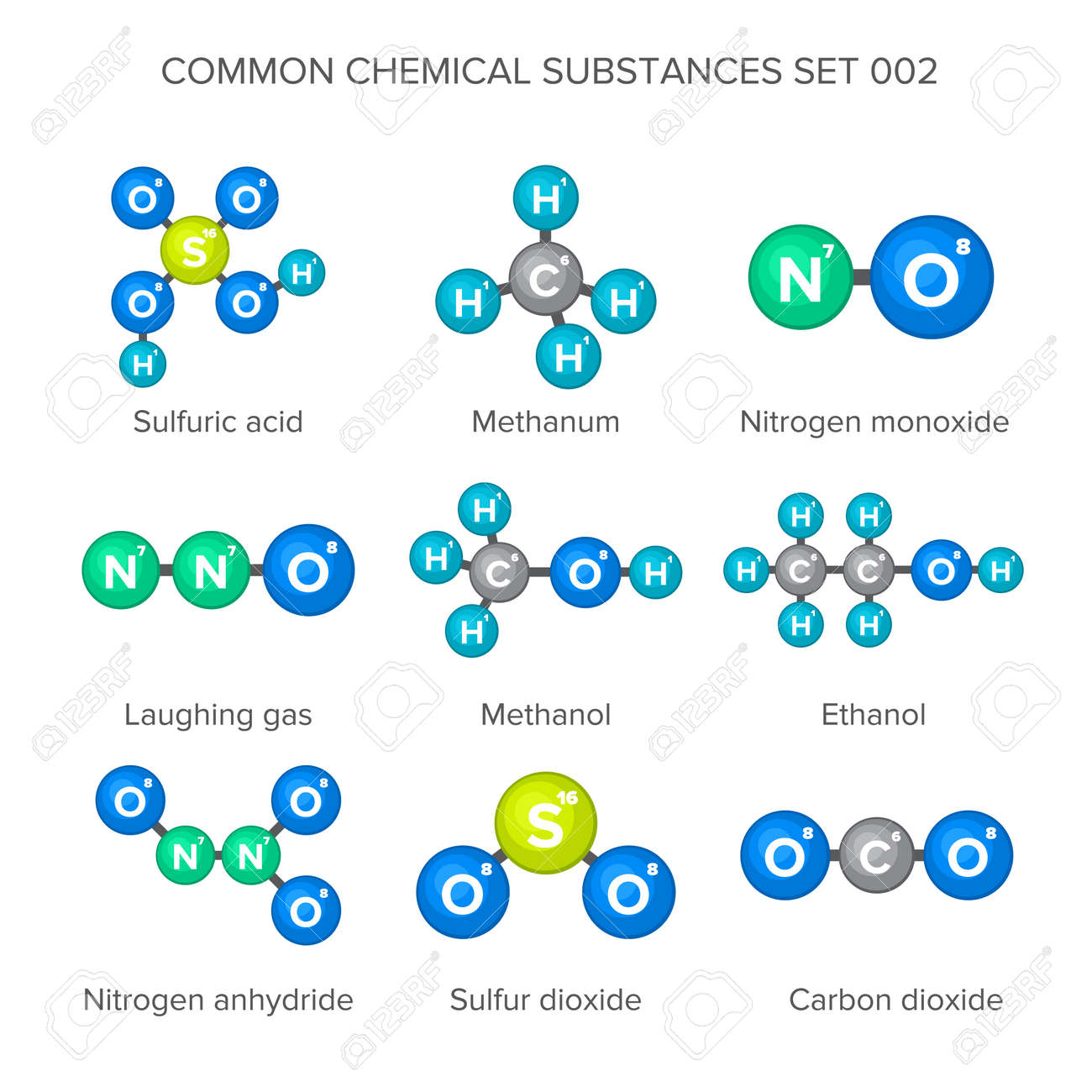
Para comprender cómo se clasifican las sustancias químicas según su estado físico, es esencial tener claridad sobre la definición y características de estas sustancias.
Las sustancias químicas son cualquier material con una composición química definida y constante. Pueden ser elementos individuales o compuestos formados por la combinación de dos o más elementos en proporciones específicas. Estas sustancias tienen propiedades químicas únicas que las distinguen y les otorgan diversas aplicaciones en la industria, la medicina, la agricultura y otros campos.
Las sustancias químicas pueden encontrarse en diferentes estados físicos, los cuales son sólido, líquido y gaseoso. Cada estado físico se caracteriza por la forma en que las partículas que componen la sustancia están dispuestas y cómo interactúan entre sí.
Características de los estados físicos de las sustancias químicas
A continuación, se detallan las principales características de cada estado físico de las sustancias químicas:
Estado sólido:
- Forma y volumen definidos: Las partículas están muy cercanas entre sí y organizadas en una estructura regular, lo que le otorga forma y volumen definidos a la sustancia.
- Incompresibilidad: Debido a la cercanía de las partículas, un sólido es prácticamente incompresible.
- Definición de límites: Los sólidos tienen límites bien definidos que los separan de otros materiales.
Estado líquido:
- Adopta la forma del recipiente: A diferencia de los sólidos, los líquidos no tienen una forma definida y adoptan la forma del recipiente que los contiene.
- Volumen constante: Aunque su forma puede cambiar, los líquidos mantienen un volumen constante.
- Fluidez: Los líquidos fluyen y pueden escurrirse debido a la capacidad de las partículas de moverse con relativa libertad.
Estado gaseoso:
- No tiene forma ni volumen definidos: Las partículas en estado gaseoso se encuentran muy separadas unas de otras y se expanden para llenar por completo el recipiente que las contiene.
- Compresibilidad: Los gases pueden comprimirse fácilmente debido a la gran separación entre partículas.
- Expansibilidad: Los gases se expanden para llenar todo el espacio disponible.
Comprender las características de los diferentes estados físicos de las sustancias químicas es fundamental para su manipulación, almacenamiento y uso adecuado en diversos procesos industriales y científicos.
Descripción detallada de los tres estados físicos de las sustancias químicas
Para comprender cómo se clasifican las sustancias químicas según su estado físico, es fundamental conocer en detalle los tres estados en los que pueden encontrarse: sólido, líquido y gaseoso.
Estado sólido:
En el estado sólido, las partículas que componen la sustancia se encuentran muy próximas unas a otras y mantienen una estructura ordenada y definida. Estas partículas vibran en su posición, pero no pueden moverse de manera significativa. Un ejemplo común de una sustancia en estado sólido es el hielo. En este estado, las moléculas de agua están unidas de manera firme y organizada, lo que le otorga una forma y volumen fijo.
Estado líquido:
En el estado líquido, las partículas tienen más libertad de movimiento que en el estado sólido, lo que les permite deslizarse unas sobre otras. Aunque siguen manteniendo cierta cohesión, no tienen una estructura ordenada como en el estado sólido. El agua en estado líquido es un ejemplo claro de esta categoría, ya que las moléculas pueden moverse con facilidad y adoptar la forma del recipiente que las contiene.
Estado gaseoso:
En el estado gaseoso, las partículas se encuentran muy separadas unas de otras y se mueven de manera aleatoria y caótica. No tienen una forma ni un volumen definido, ya que tienden a expandirse para ocupar todo el espacio disponible. El aire que respiramos es un ejemplo de una sustancia en estado gaseoso, donde las moléculas se mueven con total libertad y llenan por completo cualquier recipiente que las contenga.
Comprender los distintos estados físicos de las sustancias químicas es esencial para poder manipularlas y utilizarlas de manera adecuada en diversos procesos industriales, experimentos científicos y aplicaciones cotidianas.
Factores que influyen en el cambio de estado de las sustancias químicas
Para comprender cómo se clasifican las sustancias químicas según su estado físico, es fundamental analizar los factores que influyen en el cambio de estado de estas sustancias. Existen diversas variables que determinan si una sustancia se encuentra en estado sólido, líquido o gaseoso, y es crucial conocerlas para comprender su comportamiento y propiedades.
Temperatura y presión
La temperatura y la presión son dos factores clave que afectan directamente el estado físico de una sustancia química. Por ejemplo, el agua puede encontrarse en estado sólido (hielo), líquido (agua) o gaseoso (vapor) dependiendo de la temperatura y presión a la que se someta. Al aumentar la temperatura, las partículas de una sustancia tienden a moverse con mayor energía y, en consecuencia, pueden cambiar de estado.
Ejemplos de cambio de estado
Un ejemplo cotidiano de cómo la temperatura afecta el estado de una sustancia es el proceso de ebullición. Cuando calentamos agua a una temperatura específica, esta pasa de estado líquido a gaseoso, creando vapor. Del mismo modo, al disminuir la temperatura, el vapor de agua se condensa y vuelve a convertirse en líquido.
Diagrama de fases
Para representar gráficamente cómo cambia el estado de una sustancia en función de la temperatura y la presión, se utiliza un diagrama de fases. Este diagrama muestra las condiciones en las que una sustancia se encuentra en equilibrio entre sus distintos estados. Por ejemplo, en el caso del agua, el diagrama de fases muestra los puntos de fusión y ebullición a diferentes presiones.
Comprender los factores que influyen en el cambio de estado de las sustancias químicas es esencial para predecir su comportamiento y aplicar este conocimiento en diversos campos, desde la química hasta la ingeniería y la medicina.
Ejemplos prácticos de clasificación de sustancias según su estado físico
Para comprender mejor cómo se clasifican las sustancias químicas según su estado físico, es útil observar algunos ejemplos prácticos que ilustren esta clasificación. A continuación, se presentan casos concretos de sustancias químicas y su correspondiente estado físico:
Ejemplo 1: Agua
El agua es un ejemplo clásico de una sustancia química que puede existir en diferentes estados físicos. A temperaturas normales, el agua se encuentra en estado líquido. Sin embargo, al disminuir la temperatura lo suficiente, el agua se solidifica y se convierte en hielo (estado sólido). Por otro lado, si se aumenta la temperatura por encima de los 100 grados Celsius, el agua hierve y se convierte en vapor de agua, en estado gaseoso.
Ejemplo 2: Dióxido de carbono (CO2)
El dióxido de carbono es otro ejemplo interesante de sustancia química que puede encontrarse en diferentes estados físicos. A temperatura ambiente y presión atmosférica, el CO2 se encuentra en estado gaseoso. Sin embargo, al disminuir la temperatura lo suficiente, el dióxido de carbono se sublima y pasa directamente de estado gaseoso a estado sólido, formando lo que comúnmente conocemos como hielo seco.
Estos ejemplos prácticos demuestran cómo las sustancias químicas pueden presentarse en distintos estados físicos según las condiciones de temperatura y presión a las que estén sometidas.
Preguntas frecuentes
¿Qué es una sustancia química en estado sólido?
Es aquella que tiene forma y volumen fijos, con partículas muy cercanas y ordenadas.
¿Cómo se define una sustancia química en estado líquido?
Es aquella que tiene volumen fijo pero toma la forma del recipiente que la contiene, con partículas más separadas que en estado sólido.
¿Cuál es la característica principal de una sustancia química en estado gaseoso?
Es aquella que no tiene forma ni volumen fijos, adoptando la forma del recipiente que la contiene y con partículas muy separadas y en constante movimiento.
¿Qué es un cambio de estado en una sustancia química?
Es la transformación de una sustancia de un estado físico a otro, como de sólido a líquido (fusión) o de líquido a gas (vaporización).
¿Cuál es la importancia de clasificar las sustancias químicas según su estado físico?
Permite comprender y predecir el comportamiento de las sustancias en diferentes condiciones de temperatura y presión, así como su aplicación en diversos procesos industriales.
¿Cómo se pueden identificar los diferentes estados físicos de una sustancia química?
Mediante observación directa de sus propiedades como forma, volumen, compresibilidad y expansión, así como a través de la aplicación de cambios de temperatura y presión.
| Estado físico | Características |
|---|---|
| Sólido | Forma y volumen fijos, partículas cercanas y ordenadas. |
| Líquido | Volumen fijo, toma la forma del recipiente, partículas separadas. |
| Gaseoso | No tiene forma ni volumen fijos, partículas muy separadas y en constante movimiento. |
| Cambio de estado | Transformación de una sustancia de un estado a otro, como fusión o vaporización. |
¡Déjanos tus comentarios y revisa otros artículos relacionados con la química en nuestra página para seguir aprendiendo!